Vaccine Nano Covax được Hội đồng Đạo đức chấp thuận
Cần Thơ: Theo dõi diễn biến sức khỏe của 57 trẻ dưới 18 tuổi được tiêm vaccine / Đồng Nai thêm gần 1.000 ca mắc COVID-19 mới
Chiều 18/9, Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia đã thông qua báo cáo nghiên cứu thử nghiệm lâm sàng giữa kỳ giai đoạn 3 với
Đây là lần thứ 2 hội đồng này họp đánh giá đối với vaccine COVID-19 đầu tiên của Việt Nam hiện được thử nghiệm ở giai đoạn 3.
Vaccine Nano Covax được đánh giá là đạt yêu cầu.
Tối 18/9, GS-TS Trương Việt Dũng, Chủ tịch Hội đồng đạo đức trong nghiên cứu y sinh học Quốc gia, xác nhận vaccine Nano Covax của Công ty Nanogen đạt các yêu cầu về an toàn và tính sinh miễn dịch.
GS Dũng cho biết hội đồng chuyên môn sẽ sớm có thông tin báo chí chính thức về kết quả cuộc họp hôm nay 18/9.
Hiện toàn bộ hồ sơ, dữ liệu của vaccine Nano Covax đã được chuyển sang Hội đồng Tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc (Bộ Y tế) để tiếp tục xem xét trước khi trình Bộ Y tế đề xuất cấp giấy đăng ký lưu hành.
Đến nay, vaccine Nano Covax đã hoàn tất thử nghiệm lâm sàng giai đoạn 3 với 13.000 người tình nguyện đã tiêm đủ 2 liều vaccine.
Trước đó ngày 22/8, Hội đồng Đạo đức trong nghiên cứu y sinh học quốc gia đã họp thẩm định báo cáo giữa kỳ pha 3a của quá trình thử nghiệm lâm sàng vaccine Nano Covax, đánh giá về tính an toàn và tính sinh miễn dịch của vaccine.
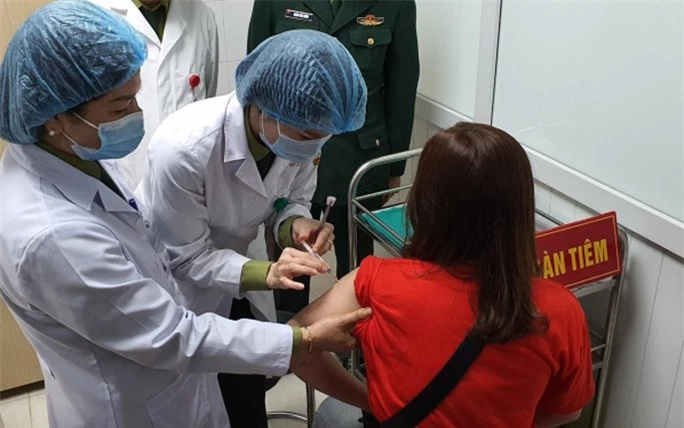
Tiêm thử nghiệm vaccine Nano Covax trên người tình nguyện
Tại cuộc họp này, Hội đồng Đạo đức quốc gia mới chỉ đánh giá báo cáo ở quy mô thử nghiệm 1.000 tình nguyện viên, với dữ liệu thu thập tính đến ngày 18/8. Hội đồng Đạo đức đánh giá vaccine Nano Covax đạt yêu cầu về tính an toàn (ngắn hạn); có tính sinh miễn dịch với virus Sar-Cov-2 chủng Vũ Hán, nhưng cần đánh giá thêm với chủng Delta (phát hiện lần đầu tại Ấn Độ) và trên chủng Alpha (phát hiện lần đầu tại Anh).
Sau đó, tại cuộc họp ngày 29/8, Hội đồng Tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc đề nghị Nanogen phối hợp với nhóm nghiên cứu bổ sung, cập nhật đánh giá tính sinh miễn dịch trên các biến chủng mới và cỡ mẫu đánh giá tính sinh miễn dịch cần thực hiện theo đúng đề cương nghiên cứu đã được thông qua.
Ngoài ra, về hiệu quả bảo vệ, hội đồng chuyên môn cũng đề nghị doanh nghiệp phối hợp với nhóm nghiên cứu để phân tích, bàn luận về mối liên quan giữa tính sinh miễn dịch của vaccine và hiệu quả bảo vệ tối thiểu 50% (theo hướng dẫn của Tổ chức Y tế thế giới - WHO) dựa trên các dữ liệu y văn.
Thời gian qua, Công ty Nanogen cùng với Học viện Quân y đã thu thập bổ sung các dữ liệu theo yêu cầu, hoàn thiện báo cáo giữa kỳ giai đoạn 3 để trình hội đồng chuyên môn.
Cách đây ít ngày, tại cuộc họp về vaccine COVID-19, ông Nguyễn Ngô Quang, Phó Cục trưởng Cục Khoa học công nghệ và Đào tạo (Bộ Y tế), Chánh Văn phòng Chương trình Quốc gia nghiên cứu phát triển vaccine, cho biết từ nay đến cuối năm 2021, Việt Nam sẽ có ít nhất 1 vaccine COVID-19 được cấp phép khẩn cấp và triển khai tiêm trong nước từ đầu năm 2022.

End of content
Không có tin nào tiếp theo









